| Descripción |
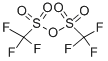
El anhídrido trifluorometanosulfónico, también conocido como anhídrido tríflico, ha demostrado ser un reactivo extraordinario para una amplia gama de transformaciones. Como reactivo comercial y fácilmente disponible, se ha utilizado ampliamente en química sintética debido a su alta electrofilia. Dada su alta afinidad hacia los O-nucleófilos, se favorece fuertemente la reacción con alcoholes, carbonilos, óxidos de azufre, fósforo y yodo para la formación de los correspondientes triflatos. Como uno de los principales grupos salientes de la química orgánica, los triflatos generados abren la puerta a diversas transformaciones posteriores, incluidas (entre otras) reacciones de sustitución, procesos de acoplamiento cruzado, reacciones redox y reordenamientos[1-2] . |
| Propiedades químicas |
Líquido transparente de incoloro a marrón claro. |
| Usos |
El anhídrido trifluorometanosulfónico es un electrófilo fuerte que se utiliza en síntesis química para introducir el grupo triflilo. |
| Usos |
El anhídrido trifluorometanosulfónico se utiliza para convertir fenoles e iminas en éster tríflico y grupo NTf. Es un electrófilo fuerte utilizado para la introducción del grupo triflilo en síntesis química. Sirve como reactivo en la preparación de triflatos de alquilo y vinilo y para la síntesis estereoselectiva de donantes de uronato de metilo de manosazida. Actúa como catalizador para la glicosilación con hidroxiazúcares anoméricos para preparar polisacáridos. |
| Definición |
ChEBI: El anhídrido tríflico es un anhídrido organosulfónico. Está funcionalmente relacionado con un ácido tríflico. |
| Perfil de reactividad |
La activación electrófila de amidas terciarias y secundarias con anhídrido tríflico (Tf2O; anhídrido rifluorometanosulfónico) en condiciones suaves da lugar a triflatos de iminio e imino, respectivamente, que podrían utilizarse como reactivos versátiles para reaccionar con diversos compuestos C, N, O y S. -nucleófilos para la transformación de una función amida en diferentes productos. Otros nucleófilos que contienen oxígeno, como los sulfóxidos y los óxidos de fósforo, también podrían sufrir un ataque nucleofílico con Tf2O para generar triflato de tionio, especies P electrófilas y triflato de fosfonio. Estas especies transitorias altamente activas podrían sufrir fácilmente reacciones de sustitución nucleofílica para otras transformaciones diversas. Además, debido a su fuerte propiedad electrófila, el Tf2O es propenso a reaccionar con nucleófilos relativamente débiles, como grupos nitrilo o algunos compuestos heterocíclicos que contienen nitrógeno. Además, el Tf2O también se ha utilizado como un reactivo eficaz de trifluorometilación y trifluorometiltiolación de radicales mediante la liberación de SO2 o un proceso de desoxigenación para la síntesis de compuestos trifluorometilados y trifluorometiltiolados [2]. |
| Peligro |
Puede ser corrosivo para los metales. Nocivo si se ingiere. Provoca quemaduras graves en la piel y daños oculares. |
| Inflamabilidad y explosibilidad |
No clasificado |
| Síntesis |
La síntesis de anhídrido trifluorometanosulfónico es la siguiente:
Un matraz de fondo redondo, seco, de {{0}} ml., se carga con 36,3 g. (0.242 moles) de ácido trifluorometanosulfónico (Nota 1) y 27,3 g. (0,192 moles) de pentóxido de fósforo (Nota 2). Se tapa el matraz y se deja reposar a temperatura ambiente durante al menos 3 horas. Durante este período, la mezcla de reacción cambia de una suspensión a una masa sólida. El matraz está equipado con un cabezal destilador de recorrido corto y se calienta primero con una corriente de aire caliente de una pistola térmica y luego con la llama de un pequeño quemador.El matraz se calienta hasta que no se destila más anhídrido trifluorometanosulfónico, pb 82-115 grados, produciendo 28,4-31,2 g. (83–91%) del anhídrido, un líquido incoloro. Aunque este producto es suficientemente puro para usarse en el siguiente paso, el ácido restante puede eliminarse del anhídrido mediante el siguiente procedimiento. Una papilla de 3,2 g. de pentóxido de fósforo en 31,2 g. del anhídrido bruto se agita a temperatura ambiente en un matraz tapado durante 18 horas. Después de equipar el matraz de reacción con un cabezal de destilación de recorrido corto, se calienta con un baño de aceite, obteniéndose 0.7 g. de antecesora, pb 74–81 grados, seguido de 27,9 g. del anhídrido del ácido trifluorometanosulfónico puro, pb 81–84 grados.

|
| almacenamiento |
Almacenar en un lugar fresco, seco y bien ventilado. Sensible a la humedad. |
| Métodos de purificación |
Se puede preparar recientemente a partir del ácido anhidro (11,5 g) y P2O5 (11,5 g, o la mitad de este peso) dejándolo a temperatura ambiente durante 1 hora, destilando los productos volátiles y luego destilándolos a través de una columna Vigreux corta. Se hidroliza fácilmente con H2O y se descompone apreciablemente después de unos días para liberar SO2 y producir un líquido viscoso. Guárdelo seco a bajas temperaturas. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referencias |
[1] Haoqi Zhang. "Anhídrido trifluorometanosulfónico en activación de amida: una herramienta poderosa para forjar núcleos heterocíclicos". TCIMAIL (2021).
[2] Dr. Qixue Qin, Prof. Dr. Ning Jiao, Zengrui Cheng. "Aplicaciones recientes del anhídrido trifluorometanosulfónico en síntesis orgánica". Angewandte Chemie 135 10 (2022). |