
Introducción del producto
| Ácido hipofosforoso Información básica |
| Descripción Propiedades químicas Usos Toxicidad IDENTIFICACIÓN DE PELIGROS Método de preparación Método de producción |
| Nombre del producto: | Ácido hipofosforoso |
| Sinónimos: | ÁCIDO HIPOFOSFOROSO, SOLUCIÓN AL 30 % (P/V); ÁCIDO HIPOFOSFOROSO, SOLUCIÓN AL 50 % (P/V); Ácido hipofosforoso: (Ácido fosfínico); Ácido hipofosforoso, solución acuosa al 50 % p/p; hipofosforoso; ácido hipofosforoso (líquido corrosivo, ácido, inorgánico, nocivo); ÁCIDO HIPOFOSFOROSO, SOLUCIÓN ACUATICA AL 50 % P/P; SOLUCIÓN DE ÁCIDO HIPOFOSFOROSO AL 50 % ACUOSO |
| Número de caso: | 6303-21-5 |
| M.F.: | HO2P |
| MW: | 63.980501 |
| Número de identificación del EINECS: | 228-601-5 |
| Categorías de productos: | HPA;Inorgánicos;6303-21-5 |
| Archivo Mol: | 6303-21-5.mol |
 |
|
| Propiedades químicas del ácido hipofosforoso |
| Punto de fusión | -25 grado |
| Punto de ebullición | 108 grados (759,8513 mmHg) |
| densidad | 1,206 g/mL a 20 grados (lit.) |
| presión de vapor | <17 mmHg ( 20 °C) |
| temperatura de almacenamiento | Sin restricciones. |
| solubilidad | Muy soluble en H2O, etanol, éter etílico. |
| PKA | pK1 1.1. |
| forma | cristales higroscópicos o líquido aceitoso incoloro |
| Color | Incoloro |
| Solubilidad en agua | SOLUBLE |
| Merck | 13,4894 |
| Estabilidad: | Estable. Incompatible con bases fuertes. Reacciona violentamente con agentes oxidantes, bases fuertes, nitrato de mercurio (II) y óxido de mercurio (II). No calentar a más de 100 °C. |
| Clave InChI | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| Referencia de la base de datos CAS | 6303-21-5(Referencia de base de datos CAS) |
| Referencia de química del NIST | Ácido hipofosforoso (6303-21-5) |
| Sistema de registro de sustancias de la EPA | Ácido fosfínico (6303-21-5) |
| Información de seguridad |
| Códigos de peligro | C |
| Declaraciones de riesgo | 34 |
| Declaraciones de seguridad | 26-36/37/39-45 |
| RIDADR | ONU 3264 8/PG 3 |
| WGK Alemania | 1 |
| RTECS (en inglés) | SZ6400000 |
| Ley de control de la contaminación del aire | Sí |
| Clase de peligro | 8 |
| Grupo de embalaje | II |
| Código HS | 28111990 |
| Datos sobre sustancias peligrosas | 6303-21-5(Datos sobre sustancias peligrosas) |
| Información de MSDS |
| Proveedor | Idioma |
|---|---|
| Ácido fosfínico | Inglés |
| Sigma Aldrich | Inglés |
| ACROS | Inglés |
| ESPARTO | Inglés |
| Uso y síntesis del ácido hipofosforoso |
| Describir | El ácido hipofosforoso también se conoce como "hipofosfito". Es un aceite incoloro o cristal delicuescente, es un importante producto químico fino. El uso principal es como agente reductor para el recubrimiento electrolítico, el fosfórico previene la decoloración de las resinas, también se puede utilizar en el catalizador de la reacción de esterificación, el refrigerante, en particular para la producción de hipofosfito de sodio, un producto de alta pureza. Existen varios métodos para su preparación, el método industrial común para su producción es el método de resina de intercambio iónico y el método de electrodiálisis. Las propiedades químicas del ácido hipofosforoso, sus usos, toxicidad y métodos de producción están editados por Andy de Chemicalbook. (2016-12-04) |
| Propiedades químicas | Se presenta en forma de cristales delicuescentes o aceite incoloro. Punto de fusión: 26,5 grados. Densidad relativa (gravedad específica): 1,439 (sólido, 19 grados). Es soluble en agua, etanol y éter, y se puede mezclar en cualquier proporción con agua, etanol y acetona. En el aire, se delicuesce fácilmente hasta convertirse en un líquido almibarado, y la solución acuosa es ácida. El ácido hipofosforoso es un ácido monobásico, en solución acuosa, el ácido hipofosforoso es un ácido fuerte, Ka=10-2 (25 grados); es relativamente estable a temperatura ambiente; la reacción de desproporción puede ocurrir a 130 grados, descomponerse en fosfina y ácido fosforoso: 2H3PO2=H3PO4+PH3 Tiene una fuerte reducción, la solución de sal de metal pesado se puede restaurar a metales como Cu2 +, Hg2 +, Ag +, como: 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ Es un oxidante débil, puede reducirse a fosfina, fosfina cuando encuentra un agente reductor fuerte. |
| Usos | 1. El ácido hipofosforoso se utiliza como agente reductor para el recubrimiento electrolítico; 2. Se puede utilizar para prevenir la decoloración de la resina de ácido fosfórico; 3. Se utiliza como catalizador de esterificación, refrigerante; 4. Se utiliza para producir hipofosfito, sales de sodio, sales de manganeso, sales de hierro se utilizan generalmente como sustancias nutritivas; 5. El ácido hipofosforoso se utiliza en medicina y como agente reductor, en la determinación de arsénico, telurio y en la separación de tantalio, niobio y otros reactivos. 6. Es un agente reductor fuerte, se puede utilizar para la preparación de hipofosfito de sodio, fosfato de calcio y otros hipofosfitos. 7. Se puede utilizar para baños de galvanoplastia. Productos farmacéuticos. Agentes reductores. Reactivos generales. 8. Es un agente reductor fuerte, se puede utilizar para hacer hipofosfito de sodio, fosfato de calcio y otros hipofosfitos. 9. Este producto es ampliamente utilizado como agente reductor, Ag, Cu, Ni, Hg y otros metales se reducen al metal correspondiente, para la verificación de As, Nb, Ta y otros reactivos, se puede utilizar para la preparación de Na, K, Ca, Mn, Fe y otros tipos de hipofosfito. |
| Toxicidad | No es combustible, pero si entra en contacto con el agente oxidante, puede provocar un incendio. Si entra en contacto con un agente oxidante, puede producirse una reacción violenta y una combustión. Si se calienta demasiado, puede descomponerse en un gas fosfina altamente tóxico o incluso explotar. Es corrosivo. El ácido hipofosforoso se añade a menudo a los refrescos y, como no se absorbe, el riesgo es pequeño, pero el hipofosfito especialmente fuerte puede causar daños gastrointestinales. Si entra accidentalmente en contacto con los ojos o la piel, se debe lavar con abundante agua. Los operarios de producción deben llevar ropa protectora y otras prendas de protección. El equipo de producción debe estar sellado y el taller debe estar bien ventilado. |
| IDENTIFICACIÓN DE PELIGROS | Indicación de peligro: Provoca graves quemaduras en la piel y daños oculares. Provoca daños oculares graves. Consejos de precaución: No respire polvo/humo/gas/niebla/vapores/aerosol. Lávese bien después de manipularlo. Use guantes protectores y protección para los ojos y la cara. EN CASO DE INGESTIÓN: Enjuagar la boca. NO provocar el vómito. EN CASO DE CONTACTO CON LA PIEL (o el cabello): quitarse inmediatamente toda la ropa contaminada. Enjuagar la piel con agua o ducharse. EN CASO DE CONTACTO CON LOS OJOS: Enjuagar cuidadosamente con agua durante varios minutos. Quitar las lentillas, si es necesario. Presente y fácil de hacer. Continúe enjuagando. EN CASO DE INHALACIÓN: Transportar a la víctima al aire libre y mantenerla en reposo en una posición cómoda para respirar. Llamar inmediatamente a un CENTRO DE TOXICOLOG A o a un médico. Tienda cerrada. Deseche este material y su recipiente en un punto de recolección de residuos peligrosos o especiales. |
| Método de preparación | 1. Se calienta la solución de fósforo e hidróxido de bario, se puede generar sal de bario Ba (H2PO2) 2 • 2H2O, se agrega ácido sulfúrico a la solución de bario de ácido hipofosforoso, Ba2+ puede precipitar: Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 El ácido hipofosforoso se puede obtener por evaporación a presión reducida y cristalización a baja temperatura. Debido a que en este proceso la solubilidad de la sal de bario es baja, la concentración del ácido hipofosforoso obtenido no es alta, por lo que el producto industrial debe purificarse por recristalización. 2. El óxido de bario (o cal) y la solución de fósforo blanco se calientan juntos para formar fosfato de bario secundario (o calcio), y luego reaccionan con ácido sulfúrico, se filtran, se concentran para obtener el producto, o la solución de hipofosfito de sodio procede de la resina de intercambio iónico de tipo H que puede derivar el producto. Este método requiere una gran cantidad de resina, y el paso de regeneración y lavado de resina es engorroso, generalmente cuesta más de $ 7 por libra, solo es adecuado para la producción de lotes pequeños y no es adecuado para aplicaciones industriales a gran escala. 3. El ácido hipofosforoso se prepara mediante el método de electrodiálisis, en el que la celda de electrodiálisis se divide en tres partes, que son la cámara del ánodo, la cámara de materia prima y la cámara del cátodo, el intermedio está separado por una membrana aniónica y una membrana catiónica, entre dos membranas se coloca una solución de hipofosfito de sodio (concentración de 100 g/L~500 g/L), la cámara del ánodo es una solución diluida de ácido hipofosforoso 5 g/L, la cámara del ánodo es una solución diluida de hidróxido de sodio (5 g/L), entre los polos se hace pasar CC (3 V~36 V), el ánodo libera oxígeno y genera un producto secundario de ácido hipofosforoso; el cátodo emite hidrógeno y genera un producto secundario de hidróxido de sodio, el tiempo de reacción es de 3~21 h. Las reacciones de la cámara del ánodo y la cámara del cátodo son las siguientes: cámara de ánodo: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 cámara catódica: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH El método de preparación de ácido hipofosforoso por electrodiálisis es simple y la inversión en equipo es pequeña, por lo que es adecuado para la producción en masa. 4. A partir del hipofosfito de sodio de grado industrial, los aniones Cl-, SO42- que afectan los indicadores de calidad del ácido hipofosforoso se eliminan por precipitación, los iones de metales pesados se eliminan de la solución formando sulfuro y luego se utiliza una resina de intercambio catiónico de ácido fuerte para obtener fosfato secundario de sodio, se puede obtener un producto de grado de alta pureza. El proceso puede producir fosfato secundario de alto grado, es técnicamente factible, el proceso es simple, de fácil operación, buena calidad del producto, puede satisfacer las necesidades de la industria electrónica, la industria de defensa y otros campos de alta tecnología. 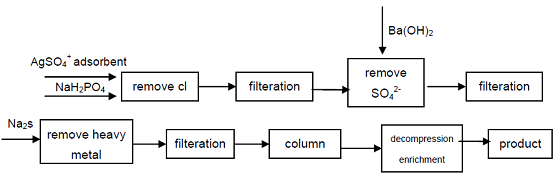 Figura 1 Proceso de producción de ácido hipofosforoso a partir de hipofosfito de sodio industrial. 5. Método de resina de intercambio iónico: aproximadamente 70 g de resina de intercambio catiónico humedecida con agua se envasa en un tubo de vidrio con ácido clorhídrico de 5 mol/L circulando aproximadamente 15 min, después de lavarlo completamente con agua, fluye a través de él una solución acuosa de hipofosfito de sodio de alta pureza (15 g/60 ml de H2O), la columna de resina se lava primero con 50 ml, luego con 25 ml de agua destilada. El ácido efluente y el lavado se combinan, se concentra por evaporación en un baño de agua. El ácido concentrado se coloca en alto vacío con un secador P205 para deshidratación, enfriamiento y cristalización, filtración, recristalización, para obtener el producto de ácido hipofosforoso. |
| Método de producción | Método de resina de intercambio iónico: coloque aproximadamente 70 g de resinas de intercambio catiónico solubles en agua para llenar un tubo de vidrio. Circule con ácido clorhídrico de 5 mol/L durante aproximadamente 15 min y lave lo suficiente con agua. Haga que una solución acuosa alta de hipofosfito de sodio (15 g/60 ml de H2O) fluya a través de la columna de resina, luego lave primero con 50 ml de agua y luego enjuague con 25 ml de agua destilada. El ácido efluente y los lavados se combinaron y se concentraron por evaporación en un baño de agua. El ácido concentrado se envía al secador P205 de alto vacío para deshidratación, seguido de cristalización por enfriamiento, filtración y recristalización para obtener el producto terminado de ácido hipofosforoso. |
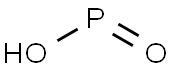
| Descripción | El ácido hipofosforoso es un potente agente reductor con una fórmula molecular de H3PO2. Los químicos inorgánicos se refieren al ácido libre con este nombre, aunque su nombre IUPAC es dihidridohidroxidooxidofosforo, o el nombre aceptable de ácido fosfínico. Es un compuesto incoloro de bajo punto de fusión, que es soluble en agua, dioxano y alcoholes. La fórmula del ácido hipofosforoso generalmente se escribe H3PO2, pero una presentación más descriptiva es HOP(O)H2 que resalta su carácter monoprótico. Las sales derivadas de este ácido se denominan fosfinatos (hipofosfitos). |
| Descripción | Este ácido tiene la fórmula general de H4P2O6 y se diferencia de los demás ácidos oxifosforosos. Tiene muchas peculiaridades. Se forma junto con los ácidos fosforoso y fosfórico, cuando el fósforo se oxida por el aire húmedo. Si el fósforo blanco se expone al aire y se agrega acetato de sodio al líquido que se forma, se separa el hipofosfato de sodio, Na2H2P2O6·6H2O, que es algo insoluble. Sin embargo, el hipofosfato de sodio monohidratado es muy soluble y delicuescente a 10,7 g/100 ml. |
| Propiedades químicas | líquido incoloro |
| Propiedades físicas | Cristales delicuescentes incoloros o líquido aceitoso; olor agrio; densidad 1,493 g/cm3; se funde a 26,5 grados; hierve a 130 grados; muy soluble en agua, alcohol y éter; la densidad de una solución acuosa al 50% es 1,13 g/mL. |
| Usos | El ácido hipofosforoso se utiliza principalmente para el niquelado electrolítico. Interviene en la reducción de sales de arenodiazonio. Actúa como aditivo en las reacciones de esterificación de Fischer. También sirve como agente neutralizante, antioxidante, catalizador en la polimerización y policondensación, y agente humectante. Además, se utiliza en la formulación de productos farmacéuticos, la decoloración de polímeros, el tratamiento de aguas y la recuperación de metales preciosos o no ferrosos. Además de esto, se utiliza como agente blanqueador para plásticos, fibras sintéticas, agente decolorante y para la estabilización del color durante la fabricación de productos químicos y varios plásticos. |
| Preparación | El ácido hipofosforoso se puede preparar mediante varios métodos: 1. Hervir fósforo blanco con hidróxido de calcio: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 La sal de calcio es soluble en agua. El tratamiento con ácido sulfúrico produce el ácido hipofosforoso: (H2correos2)2Ca+H2ENTONCES4 → 2H3correos2+ CaSO4 La mezcla de productos se filtra para eliminar el CaSO4 insoluble. La solución acuosa de ácido hipofosforoso se concentra a presión reducida. Se puede utilizar agua de barita concentrada en lugar de hidróxido de calcio. 2. Tratando el hipofosfito de sodio, NaH2PO2, con una resina de intercambio iónico. La sal de sodio se puede producir hirviendo fósforo blanco con una solución de hidróxido de sodio, una reacción similar a la del punto (1) anterior. Filipinas3 + 2I2 + 2H2O → H3correos2Hola El método descrito anteriormente puede considerarse más seguro que el que implica calentar fósforo blanco con un álcali. El ácido hipofosforoso debe almacenarse a una temperatura inferior a 50 grados. Se comercializa en forma de solución acuosa en diversas concentraciones. |
| Métodos de producción | El ácido hipofosforoso se forma por reacción del hipofosfito de bario y el ácido sulfúrico, y por filtración del sulfato de bario. Mediante la evaporación de la solución al vacío a 80 grados y luego enfriando a 0 grados, el ácido hipofosforoso cristaliza. |
| Definición | ChEBI: Oxoácido de fósforo que consiste en un solo fósforo pentavalente unido covalentemente mediante enlaces simples a dos hidrógenos y un grupo hidroxi y mediante un enlace doble a un oxígeno. El progenitor de la clase de ácidos fosfínicos. |
| Definición | Sólido cristalino blanco. Es un ácido monobásico que forma el anión H2correos2– en agua. La sal de sodio, y por lo tanto el ácido, se pueden preparar calentando fósforo amarillo con una solución de hidróxido de sodio. El ácido libre y sus sales son potentes agentes reductores. |
| Reacciones | El ácido hipofosforoso es miscible con agua en todas las proporciones y su concentración comercial es de 30% H3PO2. Los hipofosfitos se utilizan en medicina. El ácido hipofosforoso es un potente agente reductor, por ejemplo, con sulfato de cobre forma hidruro cuproso Cu2H2, precipitado marrón, que desprende gas hidrógeno y deja cobre al calentarse; con nitrato de plata produce plata finamente dividida; con ácido sulfuroso produce azufre y algo de sulfuro de hidrógeno; con ácido sulfúrico produce ácido sulfuroso, que reacciona como se indicó anteriormente; forma manganoso inmediatamente con permanganato. |
| Descripción general | El ácido hipofosforoso se presenta como un líquido oleoso incoloro o cristales delicuescentes con un olor agrio. Densidad 1,439 g/cm3. Punto de fusión 26,5 grados. La inhalación de vapores irrita o quema las vías respiratorias. El líquido y los vapores pueden irritar o quemar los ojos y la piel. |
| Reacciones del aire y el agua | Delicuescente. Soluble en agua. |
| Perfil de reactividad | El ÁCIDO HIPOFÓSFORO se descompone al calentarse y se transforma en ácido fosfórico y fosfina, que es espontáneamente inflamable. Se oxida con ácido sulfúrico y libera dióxido de azufre y azufre. Reacciona de forma explosiva con óxido de mercurio (II) [Mellor, 1940, vol. 4, 778]. Reacciona violentamente con nitrato de mercurio (II) [Mellor, 1940, vol. 4, 993]. Neutraliza bases en reacciones exotérmicas. |
| Peligro | Riesgo de incendio y explosión en contacto con agentes oxidantes. |
| Peligro para la salud | TÓXICO; la inhalación, ingestión o contacto del material con la piel puede causar lesiones graves o la muerte. El contacto con la sustancia fundida puede causar quemaduras graves en la piel y los ojos. Evite el contacto con la piel. Los efectos del contacto o la inhalación pueden ser retardados. El fuego puede producir gases irritantes, corrosivos y/o tóxicos. El agua de control o dilución del fuego puede ser corrosiva y/o tóxica y causar contaminación. |
| Peligro de incendio | No es combustible, la sustancia en sí no arde, pero puede descomponerse al calentarse y producir humos corrosivos o tóxicos. Algunos son oxidantes y pueden encender materiales combustibles (madera, papel, aceite, ropa, etc.). El contacto con metales puede generar gas hidrógeno inflamable. Los recipientes pueden explotar al calentarse. |
| Métodos de purificación | El ácido fosforoso es un contaminante común del ácido hipofosforoso comercial al 50%. Jenkins y Jones [J Am Chem Soc 74 1353 1952] purificaron este material evaporando aproximadamente 600 ml en un matraz de 1 l a 40 °C, bajo presión reducida (en N2), hasta un volumen de aproximadamente 300 ml. Después de enfriar la solución, se transfirió a un matraz Erlenmeyer de boca ancha que se tapó y se dejó en un baño de hielo seco/acetona durante varias horas para congelar (si era necesario, raspando la pared). Cuando el matraz se dejó a aproximadamente 5 °C durante 12 horas, aproximadamente el 30-40% se licuó y se filtró nuevamente. Este proceso se repitió y luego el sólido se almacenó sobre Mg(ClO4)2 en un desecador al vacío en frío. Las cristalizaciones posteriores del n-butanol disolviéndolo a temperatura ambiente y luego enfriándolo en un baño de hielo y sal a -20o no parecieron purificarlo más. El ácido libre forma cristales delicuescentes m 26,5o y es soluble en H2O y EtOH. La sal NaH2PO2 se puede purificar a través de una resina de intercambio aniónico [Klement Z Anorg Allgem Chem 260 267 1949.] |
| Productos y materias primas para la preparación del ácido hipofosforoso |
| Materias primas | AMBERLITE(R) IRC-50 |
| Productos de preparación | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->Ácido fosforoso |
Etiqueta: ácido hipofosforoso, fabricantes de ácido hipofosforoso de China, proveedores, fábrica
Artículo anterior: Bromato de potasio
Siguiente artículo: Ácido fluorobórico
También podría gustarte
Envíeconsulta



