
Introducción del producto
| Hexacloroetano Información básica |
| Descripción general Aplicación Destino ambiental Efecto sobre la salud Toxicocinética Referencias |
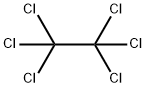
| Nombre del producto: | Hexacloroetano |
| Sinónimos: | 1,1,1,2,2,2-Hexacloroetano;Avlotano;C2Cl6;caswellno.479;CCl3CCl3;Distokal;Distopan;Distopin |
| Número de caso: | 67-72-1 |
| M.F.: | C2Cl6 |
| MW: | 236.74 |
| Número de identificación del EINECS: | 200-666-4 |
| Categorías de productos: | API Intermedio;Ordenamiento Alfa;E-L Alfabético;H;HA-HT;Volátiles/ Semivolátiles;Refrigerantes;Orgánicos;67-72-1 |
| Archivo Mol: | 67-72-1.mol |
 |
|
| Propiedades químicas del hexacloroetano |
| Punto de fusión | 183-185 grado (dec.) (lit.) |
| Punto de ebullición | 186 grados |
| densidad | 2,091 g/mL a 25 grados (lit.) |
| densidad de vapor | 8.16 (contra el aire) |
| presión de vapor | 0.4 mmHg (20 grados) |
| índice de refracción | 1.5282 (estimación) |
| Fp | 9 grados |
| temperatura de almacenamiento | 2-8 grado |
| solubilidad | Soluble en alcohol, benceno, cloroformo, éter. |
| forma | Cristales o polvo cristalino |
| Color | Blanco |
| Solubilidad en agua | 0.05 g/L (22 ºC) |
| Merck | 14,4679 |
| BRN | 1740341 |
| Constante de la ley de Henry | 1,43, 2,81 y 5,31 a 10, 20 y 30 grados, respectivamente (Munz y Roberts, 1987) |
| Límites de exposición | TLV-TWA 10 ppm (-100 mg/m3) (ACGIH), 1 ppm (MSHA y OSHA), límite mínimo factible (NIOSH); carcinogenicidad: evidencia limitada en animales (IARC). |
| Estabilidad: | Estable. No combustible. Puede reaccionar con metales calientes y agentes oxidantes fuertes. |
| Referencia de la base de datos CAS | 67-72-1(Referencia de base de datos CAS) |
| Referencia de química del NIST | Etano, hexacloro-(67-72-1) |
| CIIC | 2B (Vol. 73) 1999 |
| Sistema de registro de sustancias de la EPA | Hexacloroetano (67-72-1) |
| Información de seguridad |
| Códigos de peligro | Xn,N,V,F |
| Declaraciones de riesgo | 40-51/53-36/37/38-39/23/24/25-36/38-23/24/25-11-50/53-52/53 |
| Declaraciones de seguridad | 36/37-61-45-36/37/39-26-24-16-7-37/39 |
| RIDADR | ONU 9037 |
| OEB | B |
| LEO | TWA: 1 ppm (10 mg/m3) [piel] (cloroetanos) |
| WGK Alemania | 3 |
| RTECS (en inglés) | KI4025000 |
| Ley de control de la contaminación del aire | Sí |
| Clase de peligro | 9 |
| Grupo de embalaje | III |
| Código HS | 29031990 |
| Datos sobre sustancias peligrosas | 67-72-1(Datos sobre sustancias peligrosas) |
| Toxicidad | MLD iv en perros: 325 mg/kg (Barsoum, Saad) |
| IDLA | 300 ppm |
| Información de MSDS |
| Proveedor | Idioma |
|---|---|
| Sigma Aldrich | Inglés |
| ACROS | Inglés |
| ESPARTO | Inglés |
| Uso y síntesis del hexacloroetano |
| Descripción general | El hexacloroetano (HCE; CASRN 67-72-1) es un hidrocarburo halogenado que consta de seis cloros unidos a una cadena principal de etano. En el pasado, el HCE se utilizaba como antihelmíntico para el tratamiento de las duelas de las ovejas, pero ya no se utiliza con este fin desde que la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) retiró la aprobación para este uso en 1971.[1]El HCE se utiliza principalmente en el ámbito militar para bombas de humo, granadas de humo y dispositivos pirotécnicos.[1]El HCE también se ha utilizado como aditivo de polímeros, repelente de polillas, plastificante para ésteres de celulosa y disolvente de insecticidas, y en metalurgia para refinar aleaciones de aluminio.[1, 3]También se identificó HCE en el espacio libre de productos domésticos que contenían blanqueador con cloro.[4].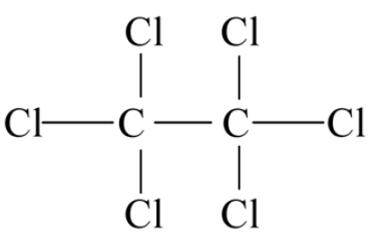 Figura 1. Estructura química del hexacloroetano. El HCE se produce mediante la cloración de tetracloroetileno (PERC) en presencia de cloruro férrico.[1]. HCE se produjo en los Estados Unidos (EE. UU.) para distribución comercial desde 1921 hasta 1967, pero actualmente no se distribuye comercialmente.[1, 5]En la década de 1970, los productores estadounidenses de HCE informaron que el HCE no se distribuía, sino que solo se utilizaba internamente o se reciclaba.[1]Los distribuidores estadounidenses en la década de 1970 importaron HCE de Francia, España y el Reino Unido.[1]La producción estadounidense más las importaciones de HCE totalizaron entre 10 y 50 millones de libras en 1986, entre 1 y 10 millones de libras en 1990, entre 10 y 50 millones de libras en 1994, entre 500 y 1 millón de libras en 1998, entre 10 y 500 libras en 2002 y entre 1 y 10 millones de libras en 2006.[6]. |
| Solicitud | Se informó que el hexacloroetano se utilizaba como intermediario químico, como agente fundente para el refinado de granos y la desgasificación de aleaciones de aluminio, y como retardante de llama en resinas de laminación industriales. También se informó que se utilizaba como reactivo en municiones de humo militares. Otros usos del hexacloroetano mencionados en la literatura científica y técnica anterior fueron en pirotecnia militar, en la industria metalúrgica, como plastificante, como supresor de ignición, como auxiliar de procesamiento en varios procesos industriales, como componente de formulaciones fungicidas e insecticidas y (anteriormente) como antihelmíntico en medicina veterinaria.[1, 7]El uso de hexacloroetano en cosméticos aparece en la Lista de ingredientes cosméticos prohibidos y restringidos (más comúnmente conocida como la Lista de ingredientes cosméticos prohibidos o simplemente la Lista de ingredientes), una herramienta administrativa que los países occidentales utilizan para comunicar a los fabricantes y otros que ciertas sustancias, cuando están presentes en un cosmético, pueden contravenir (a) la prohibición general que se encuentra en la sección 16 de la Ley de Alimentos y Medicamentos o (b) una disposición de las Regulaciones de Cosméticos. El hexacloroetano no se utiliza en formulaciones de pesticidas en los países occidentales. Además, actualmente en los países occidentales, el hexacloroetano no está presente en productos veterinarios, ya no se utiliza en municiones de humo militares y no se ha encontrado evidencia de su uso actual como retardante de llama. El hexacloroetano no es un aditivo alimentario aprobado en los países occidentales y no estaba presente en varias bases de datos de alimentos regulatorios.[8, 9]Sin embargo, sigue importándose a los países occidentales para su uso como agente desgasificador para la eliminación de óxidos e hidrógeno de las aleaciones de aluminio durante la fundición a presión en una cantidad inferior a 2000 kg al año. La producción y el uso del hexacloroetano se están eliminando gradualmente a nivel internacional. La Comisión Europea prohíbe el uso de hexacloroetano en la fabricación o el procesamiento de metales no ferrosos[10]En los Estados Unidos, se ha producido una tendencia a abandonar el uso de fundente de hexacloroetano en la industria del aluminio secundario.[11]De manera similar, los representantes de la industria del aluminio en los Estados Unidos informan que el hexacloroetano ya no se utiliza en la mayoría de los procesos de desgasificación del aluminio primario.[12]La Asociación del Aluminio de los países occidentales también ha informado que sus miembros no utilizan hexacloroetano en sus actividades (industria del aluminio primario). Se informó que el hexacloroetano puede ser un componente de grasas y aceites lubricantes, compuestos de calafateo y selladores no estructurales, productos químicos automotrices, productos para el lavado y planchado de ropa y agentes de limpieza en seco, pero no se proporcionaron datos cuantitativos.[13]. |
| Destino ambiental | El hexacloroetano es una sustancia química industrial cuya presencia en la naturaleza no se conoce. No se produce para su distribución comercial en los Estados Unidos, sino que se importa para su uso en dispositivos pirotécnicos y de humo militares y como intermediario en la industria de sustancias químicas orgánicas. Se libera al medio ambiente a partir de estos usos, principalmente a la atmósfera. El hexacloroetano es relativamente persistente en el medio ambiente. Se volatiliza fácilmente del agua a la atmósfera, con una vida media de menos de un día en algunas aguas. El hexacloroetano también puede filtrarse a través del suelo a las aguas subterráneas. No se espera que la hidrólisis ni la fotólisis sean procesos de eliminación importantes, pero el hexacloroetano puede reducirse en sistemas acuáticos en presencia de agentes específicos. Se ha informado de bioconcentración en peces, pero es poco probable que se produzca una biomagnificación a través de la cadena alimentaria. La biodegradación puede contribuir a la eliminación del hexacloroetano de las aguas ambientales, pero hay pruebas contradictorias sobre la importancia de este proceso de destino para el hexacloroetano. Se ha detectado hexacloroetano en niveles bajos (ng/m3) en la atmósfera y, ocasionalmente, en sistemas de agua potable. Rara vez se detecta en aguas superficiales o en la biota, y no se ha informado de su presencia en el suelo, los sedimentos ni en productos alimenticios comerciales. Se ha identificado hexacloroetano en al menos 45 de los 1.416 sitios de desechos peligrosos que se han propuesto para su inclusión en la Lista Nacional de Prioridades (NPL) de la EPA (HazDat 1995). Sin embargo, se desconoce el número de sitios evaluados para la presencia de hexacloroetano. |
| Efecto sobre la salud | Puede producirse una leve irritación de la piel cuando los trabajadores de una fábrica de municiones estuvieron expuestos a niveles bajos de hexacloroetano.[15]Los trabajadores deben usar ropa protectora para reducir en gran medida la exposición. Según los datos obtenidos con animales, el hexacloroetano en el aire puede irritar la nariz y los pulmones de los seres humanos y provocar una acumulación de mucosidad en la nariz, muy similar a una alergia. También puede irritar los ojos y hacer que lagrimeen. Las personas que se encuentran en un área donde hay mucho vapor de hexacloroetano pueden tener contracciones en los músculos faciales o dificultad para moverse.[15]Estos efectos se han observado en animales durante la exposición a niveles mucho mayores que los encontrados en el uso industrial del hexacloroetano o los que se esperarían en áreas cercanas a un sitio de desechos peligrosos. El hexacloroetano no es una sustancia altamente tóxica. Las personas que se exponen a una gran cantidad durante un largo tiempo pueden tener sus células hepáticas destruidas y grasa acumulada en su hígado. También existe una pequeña posibilidad de que los riñones puedan resultar dañados[15]. Aunque ningún resultado de estudios en animales sugiere que el hexacloroetano le dificultaría quedar embarazada o que dañaría a su bebé durante el embarazo, los estudios en animales que han analizado los efectos del hexacloroetano durante el embarazo son limitados.[15]. Los tumores hepáticos pueden desarrollarse en ratones que estuvieron expuestos por vía oral al hexacloroetano durante toda su vida. Los tumores hepáticos son comunes en ratones. El hexacloroetano puede no tener necesariamente el mismo efecto en las personas. Las ratas macho que estuvieron expuestas al hexacloroetano durante toda su vida desarrollaron tumores renales. Este tipo de tumor no se encuentra en las personas, por lo que es poco probable que la exposición al hexacloroetano provoque cáncer de riñón. El Departamento de Salud y Servicios Humanos afirma que se puede prever razonablemente que el hexacloroetano sea un carcinógeno (puede causar cáncer). La Agencia Internacional para la Investigación del Cáncer (IARC) ha determinado que el hexacloroetano no es clasificable en cuanto a su carcinogenicidad en las personas. La EPA ha determinado que el hexacloroetano es un posible carcinógeno humano.[15]. |
| Toxicocinética | No hay estudios que hayan evaluado la absorción de HCE en humanos por exposición oral o por inhalación. Se identificó HCE en el líquido folicular de mujeres sometidas a fertilización in vitro (FIV) durante un análisis de contaminantes ambientales.[16]Estos datos indican el potencial de absorción de HCE, pero no la fuente o vía de exposición. La tasa de absorción dérmica de HCE se ha descrito como limitada.[1]; la absorción de una solución saturada de HCE a través de la piel humana se estimó en 0.023 mg/cm2•hora[17]Existen datos limitados sobre la distribución de HCE en humanos.[16]Los estudios en animales han demostrado consistentemente que el HCE se distribuye a la grasa, los riñones, el hígado y la sangre.[18, 19]Los datos de estudios in vivo e in vitro respaldan la conclusión de que el metabolismo de la HCE es incompleto y que la HCE no metabolizada se excreta en el aire exhalado y posiblemente en la orina. Los datos del metabolismo in vivo de la HCE se limitan a tres estudios: Mitoma et al. (1985) en ratas y ratones[20]; Jondorf et al. (1957) en conejos[21]; y Fowler (1969) en ovejas[22]Cada uno de estos estudios sugiere un metabolismo limitado de la HCE. También se han identificado diversos metabolitos intermediarios en el aire exhalado y la orina.[21, 22]Los estudios in vitro realizados con microsomas hepáticos indicaron que el metabolismo del HCE involucra enzimas del citocromo P450 (CYP450) inducibles por fenobarbital.[23, 24]; sin embargo, no se han identificado enzimas específicas. Las enzimas CYP450 inducidas por el fenobarbital incluyen las de las subfamilias 2A, 2B, 2C y 3A. Un estudio[25]Se encontró evidencia de la participación del CYP1A2 en el metabolismo de la HCE, aunque esto no fue respaldado por los resultados de estudios in vitro con 3-metilcolantreno, un inductor de la subfamilia CYP450 1[23, 24]No hay estudios disponibles que hayan evaluado la eliminación del HCE en humanos. Los estudios realizados en animales indicaron que las principales vías de eliminación del HCE son la materia fecal o el aire exhalado.[20-22]Estudios sobre ovejas[22]indicó que el HCE administrado por vía oral se elimina por vía fecal sin absorción ni metabolismo, mientras que los estudios con roedores[20]Se ha demostrado que el HCE se absorbe y se elimina por exhalación. Se desconoce por qué hay una diferencia en la eliminación entre ovejas y roedores. |
| Referencias |
ATSDR (Agencia para Sustancias Tóxicas y Registro de Enfermedades). (1997). Perfil toxicológico del hexacloroetano. Atlanta, GA: Departamento de Salud y Servicios Humanos de los Estados Unidos. ACGIH (Conferencia Americana de Higienistas Industriales Gubernamentales). (2001). Documentación de valores límite de umbral para sustancias químicas y agentes físicos e índices de exposición biológica para 2001. Cincinnati, OH. Agencia de Protección Ambiental de los Estados Unidos (US EPA, por sus siglas en inglés). (1991). Alfa-globulina α-β: asociación con toxicidad renal inducida químicamente y neoplasia en ratas macho. (EPA/625/3-91/019F). págs. 136. Washington, DC: Agencia de Protección Ambiental de los Estados Unidos, Foro de Evaluación de Riesgos. Odabasi, M. (2008). Environ Sci Technol 42: 1445-1451 IARC. (Agencia Internacional para la Investigación sobre el Cáncer). (1979). Algunos hidrocarburos halogenados: resumen de los datos notificados y evaluación. En Monografías de la IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos. Lyon, Francia. NTP. (Programa Nacional de Toxicología). (2011). Informe sobre carcinógenos. Washington, DC: Departamento de Salud y Servicios Humanos de los Estados Unidos. [IARC] Grupo de trabajo de la IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos. 1999. Algunas sustancias químicas que causan tumores en los riñones o la vejiga urinaria en roedores y algunas otras sustancias. IARC Monogr Eval Carcinogen Risk Chem Hum 73: 295-306. [FDA] Administración de Alimentos y Medicamentos. 2013a. Todo lo que se añade a los alimentos en los Estados Unidos. [FDA] Administración de Alimentos y Medicamentos. 2013a. Lista de aditivos indirectos utilizados en sustancias en contacto con alimentos. [CEC] Comisión de las Comunidades Europeas. 2001. Directiva 2001/91/CE de la Comisión, de 29 de octubre de 2001. Strueter RP. 1999. Comentarios recibidos de la Asociación del Aluminio por el Sr. Frank Anscombe, Agencia de Protección Ambiental de los EE. UU., Chicago, IL, 25 de febrero de 1999. [CGLI] Consejo de Industrias de los Grandes Lagos. 1999. Octacloroestireno y fuentes industriales sugeridas. Informe para el Grupo de Trabajo de la Estrategia Binacional de Sustancias Tóxicas de los Grandes Lagos (OCS), 9 de marzo de 1999. Scorecard[base de datos en Internet]. 2005. Perfil químico del hexacloroetano (Número CAS: 67-72-1). HazDat. 1995. Agencia para Sustancias Tóxicas y el Registro de Enfermedades (ATSDR), Atlanta, GA. 9 de marzo de 1993. https://www.atsdr.cdc.gov/phs/phs.asp?id=868&tid=169 Younglai, E; y otros (2002). Arch Environ Contam Toxicol 43: 121-126. Fiserova-Bergerova, V y otros (1990) Am J Ind Med 17: 617-635 Gorzinski, S y otros (1985). Fármaco químico Toxicol 8: 155-169 Nolan, R y Karbowski, R. (1978). Hexacloroetano: eliminación y distribución tisular en ratas Fischer 344. (878213746). Midland, MI: Dow Chemical Company, Toxicology Research Laboratory. Mitoma, C; (1985) et al Droga Químico Toxicol 8: 183-194. Jondorf, W; (1957) et al Biochem J 65: 14P-15P. Fowler, J. (1969). Br J Pharmacol 35: 530-542. Nastainczyk, W; y otros (1982a). Biochem Pharmacol 31: 391-396. Nastainczyk, W; et al (1982b). En R Snyder (Ed.), Intermedios reactivos biológicos II: Mecanismos químicos y efectos biológicos (Vol. 136 Pt. A, pp. 799-808). Nueva York, NY: Plenum Press. Yanagita, K y otros (1997). Arch Biochem Biophys 346: 269-276. |
| Descripción | El hexacloroetano (HCE) es un hidrocarburo halogenado que consiste en seis cloros unidos a un etano (ACGIH, 1991); es un sólido de color blanco a amarillo pálido que es inestable en el aire y se evapora gradualmente. Huele a alcanfor cuando su concentración en el aire y el agua es de 150 y 10 ppb, respectivamente. El HCE en sí no se incendia fácilmente; sin embargo, en condiciones acuosas no biológicas se ha determinado que el HCE es inestable y se produce una decloración no enzimática en ausencia de nicotinamida adenina dinucleótido fosfato (NADP). Se degrada rápidamente en el suelo o en las aguas subterráneas. Además, algunos microorganismos descomponen el HCE sin oxígeno, y se ha informado de su descomposición en condiciones aeróbicas. Se ha determinado cierta bioconcentración de HCE en los peces, aunque los niveles superiores a lo largo de la cadena alimentaria son limitados, ya que los peces lo metabolizan rápidamente, lo que se analiza más adelante (ATSDR, 1997). Se ha propuesto que los ojos, la piel, el sistema respiratorio y los riñones son los principales objetivos en humanos tras la exposición. Los síntomas incluyen parpadeo, lagrimeo, fotofobia e irritación de los ojos. Además, los músculos faciales pueden tener dificultad para moverse. Los estudios en animales sobre los efectos del HCE durante el embarazo son limitados. Después de la exposición oral, el HCE se distribuye principalmente al tejido graso. Los estudios toxicocinéticos en animales indicaron que el HCE se localiza y metaboliza principalmente en el hígado y el riñón. Varios metabolitos correspondientes han demostrado toxicidades hepáticas y renales similares a la del HCE. Se observaron efectos neurológicos como temblores y ataxia en perros Beagle, ratas y ratas preñadas. Otros efectos a través de la exposición por inhalación incluyeron reducción del peso corporal y aumento del peso relativo del hígado en ratas y cobayas. En otro estudio, las ratas macho también mostraron un aumento del peso relativo del bazo y los testículos. Con base en la Proposición 65 de California, se propuso que el HCE es carcinógeno para los humanos e induce tumores en sitios distintos del sitio de entrada. Los efectos no cancerosos incluyen degeneración renal (nefropatía tubular, necrosis del epitelio tubular renal, formación de gotitas hialinas, regeneración tubular y cilindros tubulares) y necrosis hepatocelular. Produce nefropatía por gotitas hialinas y toxicidad renal, e induce segregación cromosómica deficiente, letalidad y detención del crecimiento mitótico (Crebelli et al., 1995, 1992, 1988). |
| Propiedades químicas | polvo cristalino blanco |
| Propiedades químicas | El hexacloroetano es un sólido blanco con un olor parecido al del alcanfor. Se evapora gradualmente cuando se expone al aire. |
| Propiedades físicas | Cristales rómbicos, triclínicos o cúbicos, incoloros y con olor similar al alcanfor. La concentración umbral del olor es de 1,15 ppm (citado por Amoore y Hautala, 1983). |
| Usos | El hexacloroetano se utiliza como disolvente en fuegos artificiales y dispositivos de humo, en explosivos, en celuloide, como insecticida y como acelerador de vulcanización del caucho. Anteriormente se utilizaba como antihelmíntico para el ganado. El hexacloroetano es un agente clorante muy eficaz en la preparación de clorosilanos a partir de hidrosilanos. |
| Usos | En metalurgia, para refinar aleaciones de aluminio, eliminar impurezas de metales fundidos, recuperar metal de minerales o productos de fundición. Agente desgasificador de magnesio; para inhibir la explosividad del metano y la combustión del perclorato de amonio. Generador de humo en granadas; en pirotecnia. Supresor de ignición, en líquidos extintores de incendios, aditivo para polímeros, agente ignífugo, agente vulcanizante. En la producción de diamantes sintéticos. |
| Usos | Las aplicaciones del hexacloroetano han sido extensas; sin embargo, los usos industriales están disminuyendo. El hexacloroetano se utiliza principalmente en municiones fumígenas militares (por ejemplo, botes de humo, granadas, cartuchos y proyectiles utilizados para generar "humo" o "niebla") y en pirotecnia. El uso anual promedio estimado de hexacloroetano entre 1966 y 1977 en una importante planta de fabricación de dispositivos pirotécnicos y de humo fue de 192.802 libras. En la década de 1970, aproximadamente la mitad del hexacloroetano distribuido se utilizó para fabricar dispositivos pirotécnicos y generadores de humo militares, entre el 30% y el 40% para fabricar pastillas desgasificadoras para eliminar las burbujas de aire del mineral fundido en las fundiciones de aluminio, y entre el 10% y el 20% como antihelmíntico para controlar las duelas del hígado en las ovejas y el ganado. La Administración de Alimentos y Medicamentos de los Estados Unidos retiró la aprobación para el uso de hexacloroetano como antihelmíntico en 1971, y probablemente ya no se utiliza para este propósito (ATSDR 1997). Su uso para desgasificar aluminio también se ha eliminado casi por completo en los Estados Unidos (EPA 1999). Otros usos en metalurgia incluyen el refinamiento de aleaciones, la eliminación de impurezas de metales fundidos, la recuperación de metales de minerales o productos de fundición y como agente desgasificador para el magnesio; sin embargo, la Unión Europea comenzó a eliminar gradualmente el uso de hexacloroetano en metales no ferrosos en 1998 (CE 1998). Se han identificado otros usos anteriores del hexacloroetano, pero muchos de ellos probablemente se han interrumpido o implican el uso de cantidades limitadas. El hexacloroetano se utiliza como sustancia química de laboratorio y como ingrediente en diversas formulaciones fungicidas e insecticidas, lubricantes de presión extrema y plásticos (ATSDR 1997, IARC 1999, HSDB 2009). Otros usos anteriores incluyen como repelente de polillas y en la industria química como aditivo de polímeros, plastificante para ésteres de celulosa, acelerador, agente vulcanizante, disolvente de procesos en la fabricación de caucho, retardante en procesos de fermentación y componente de pinturas submarinas, y en la producción de algunos tipos de diamantes sintéticos. También se ha utilizado como componente de fluidos extintores de incendios, aditivo en líquidos combustibles (supresor de ignición) e inhibidor de la explosividad del metano y de la combustión del perclorato de amonio (IARC 1979, 1999, HSDB 2009). |
| Definición | ChEBI: Un miembro de la clase de cloroetanos que es el etano en el que todos los hidrógenos son reemplazados por grupos cloro. |
| Descripción general | El hexacloroetano es un sólido cristalino incoloro con un olor parecido al del alcanfor. El hexacloroetano puede provocar enfermedades por inhalación o ingestión y puede irritar la piel, los ojos y las membranas mucosas. Cuando se calienta a altas temperaturas, el hexacloroetano puede emitir humos tóxicos. El principal peligro es la amenaza para el medio ambiente. Se deben tomar medidas inmediatas para limitar su propagación al medio ambiente. El hexacloroetano se utiliza para fabricar otros productos químicos. |
| Reacciones del aire y el agua | Insoluble en agua. |
| Perfil de reactividad | El hexacloroetano puede reaccionar con hierro, zinc y aluminio calientes. La deshalogenación del hexacloroetano por reacción con álcalis y metales producirá cloroacetilenos inestables. El hexacloroetano también puede reaccionar con agentes oxidantes fuertes. |
| Peligro | Tóxico por ingestión e inhalación, fuerte irritante, se absorbe por la piel. Posible carcinógeno. |
| Peligro para la salud | El compuesto es un potente narcótico y veneno hepático; también puede causar cambios en la composición sanguínea y trastornos neurológicos. La exposición repetida por inhalación puede ser fatal. La ingestión causa vómitos, diarrea, daño grave a las mucosas, necrosis hepática, cianosis, pérdida de conocimiento, pérdida de reflejos y muerte. El contacto con los ojos causa irritación y lagrimeo. Puede absorberse a través de la piel y puede producir lesiones cutáneas graves. |
| Peligro para la salud | Los vapores de hexacloroetano son irritantes para los ojos y las mucosas. Dosis orales de 1000 mg/kg produjeron debilidad, marcha tambaleante y espasmos musculares en perros. Los conejos alimentados con 1000 mg/kg durante 12 días desarrollaron necrosis; una cantidad menor, 320 mg/kg, causó degeneración hepática; no se observaron efectos con una dosis de 100 mg/kg (Weeks 1979). La toxicidad aguda por inhalación es de orden bajo en animales. Los efectos tóxicos subagudos en perros expuestos a vapores de hexacloroetano de 260- ppm durante 6 horas al día, 5 días a la semana durante 6 semanas fueron temblores, ataxia, hipersalivación, balanceo de la cabeza y fasciculaciones musculares faciales (Weeks 1979). La concentración letal en ratas es de 5900 ppm a partir de una exposición de 8- horas. Valor LD50, oral (ratas): 4460 mg/kg Las pruebas de mutagenicidad y teratogenia dieron resultados negativos. El potencial carcinógeno del hexacloroetano se observó en animales de prueba sólo en dosis extremadamente altas administradas de forma continua durante un largo período de tiempo (ACGIH 1986). Provocó tumores hepáticos en ratones. |
| Peligro de incendio | Peligros especiales de los productos de combustión: En caso de incendio, puede formarse vapor irritante de cloruro de hidrógeno. |
| Posible exposición | En los EE. UU., aproximadamente la mitad del HCE se utiliza en el ejército para dispositivos que producen humo. También se utiliza para eliminar burbujas de aire en el aluminio fundido. Puede estar presente como ingrediente en algunos fungicidas, insecticidas, lubricantes y plásticos. Ya no se fabrica en los Estados Unidos, pero se forma como subproducto en la producción de algunos productos químicos. Puede formarse en incineradores cuando se queman materiales que contienen hidrocarburos clorados. También se puede formar algo de HCE cuando el cloro reacciona con compuestos de carbono en el agua potable. Como medicamento, el HCE se utiliza como antihelmíntico para tratar la fascioliasis en ovejas y ganado. También se añade al pienso de los rumiantes, evitando la metanogénesis y aumentando la eficiencia alimenticia. El HCE se utiliza en la producción de metales y aleaciones, principalmente en el refinado de aleaciones de aluminio. También se utiliza para eliminar impurezas de metales fundidos, recuperar metales de minerales o productos de fundición y mejorar la calidad de varios metales y aleaciones. El HCE está contenido en pirotecnia. Inhibe la explosividad del metano y la combustión del perclorato de amonio. El humo que contiene HCE se utiliza para extinguir incendios. El HCE tiene diversas aplicaciones como aditivo para polímeros. Tiene propiedades ignífugas, aumenta la sensibilidad a la reticulación por radiación y se utiliza como agente vulcanizante. Añadido a las fibras de polímeros, el HCE actúa como agente de hinchamiento y aumenta la afinidad por los colorantes. |
| Primeros auxilios | Si esta sustancia química entra en contacto con los ojos, quítese inmediatamente los lentes de contacto y láveselos inmediatamente durante al menos 15 minutos, levantando ocasionalmente los párpados superior e inferior. Busque atención médica de inmediato. Si esta sustancia química entra en contacto con la piel, quítese la ropa contaminada y lávese inmediatamente con agua y jabón. Busque atención médica de inmediato. Si se ha inhalado esta sustancia química, retírese de la zona de exposición, comience a realizar respiración artificial (utilizando las precauciones universales, incluida una máscara de reanimación) si se ha detenido la respiración y reanimación cardiopulmonar (RCP) si se ha detenido el corazón. Traslade de inmediato a un centro médico. Si se ha ingerido esta sustancia química, busque atención médica. Déle agua en grandes cantidades e induzca el vómito. No haga vomitar a una persona inconsciente. |
| Carcinogenicidad | Se prevé razonablemente que el hexacloroetano sea cancerígeno basándose en evidencia suficiente de carcinogenicidad en seres humanos a partir de estudios en animales de experimentación. |
| Destino ambiental | Biológico.En condiciones aeróbicas o en sistemas experimentales que contienen cultivos mixtos, se ha informado de que el hexacloroetano se degrada a tetracloroetano (Vogel et al., 1987). En una suspensión acuosa anóxica desinhibida, el hexacloroetano se degrada a tetracloroetileno. La vida media informada para esta transformación fue de 19,7 min (Jafvert y Wolfe, 1987). Cuando se incubó estáticamente hexacloroetano (5 y 10 mg/L) en la oscuridad a 25 grados con extracto de levadura e inóculo de aguas residuales domésticas sedimentadas durante 7 días, se observó una biodegradación del 100% con una rápida adaptación (Tabak et al., 1981). Fotolítico.Cuando una solución acuosa que contenía hexacloroetano se fotooxidó con luz ultravioleta a 90–95 grados, el 25, el 50 y el 75 % se degradó a dióxido de carbono después de 25,2, 93,7 y 172,0 h, respectivamente (Knoevenagel y Himmelreich, 1976). Químico/Físico.La vida media de hidrólisis informada a 25 grados y pH 7 es 1,8 x 109año (Jeffers et al., 1989). No se observó hidrólisis después de 13 días a 85 grados y valores de pH de 3, 7 y 11 (Ellington et al., 1987). De manera similar, no se observó hidrólisis medible en condiciones neutras y alcalinas (Jeffers y Wolfe, 1996). |
| almacenamiento | Código de color: azul: peligro para la salud/veneno: almacenar en un lugar seguro para evitar el envenenamiento. Antes de trabajar con este producto químico, debe recibir capacitación sobre su manipulación y almacenamiento adecuados. El hexacloroetano debe almacenarse para evitar el contacto con hierro caliente, zinc, aluminio y álcalis, ya que se producen reacciones violentas. Almacene en recipientes bien cerrados en un área fresca y bien ventilada, lejos del calor. Se debe establecer un área regulada y marcada donde se manipule, use o almacene este producto químico de conformidad con la Norma 1910.1045 de OSHA. |
| Envío | UN2811 Sólidos tóxicos, orgánicos, nos, Clase de peligro: 6.1; Etiquetas: 6.1-Materiales venenosos, Nombre técnico requerido. UN3077 Sustancias ambientalmente peligrosas, sólidas, nos, Clase de peligro: 9; Etiquetas: 9-Material peligroso misceláneo, Nombre técnico requerido. |
| Métodos de purificación | Destilarlo al vapor y luego cristalizarlo en EtOH al 95 %. Secarlo en la oscuridad al vacío. [Beilstein 1 IV 148.] |
| Evaluación de toxicidad | Los informes sobre los efectos en la salud humana son limitados y se ven afectados por la coexposición a múltiples solventes u otros tóxicos (por ejemplo, humo de óxido de cinc y HCE), y son demasiado pequeños para proporcionar conclusiones definitivas sobre los efectos en la salud. Los estudios realizados en animales sugieren que el HCE se metaboliza principalmente a tetracloroetileno (PERC) y pentacloroetano por las enzimas CYP450 del hígado, con un probable metabolismo posterior a TCE. Los metabolitos identificados en la orina incluyen TCA, tricloroetanol, ácido oxálico, dicloroetanol, ácido dicloroacético y ácido monocloroacético (Gorzinski et al., 1985). Los estudios de TCA (un metabolito potencial de HCE) indican que la generación de radicales libres puede desempeñar un papel en la mediación de la toxicidad, particularmente en el hígado. Sin embargo, no hay datos disponibles que demuestren la generación de radicales libres después de la exposición a HCE, y se desconoce si el HCE inalterado o sus metabolitos son responsables de las toxicidades hepáticas y renales observadas en estudios animales. Se informó de peroxidación lipídica por formación de malondialdehído y dienos conjugados, que involucra radicales libres (Town et al., 1984). En otro estudio, la presencia de carbono radiomarcado medido por estudios de unión in vivo sugirió que HCE puede unirse al ADN, ARN y proteínas. Por lo tanto, la toxicidad renal y la hepatotoxicidad también pueden involucrar la unión de HCE al ADN, ARN o proteínas, lo que resulta en citotoxicidad y contribuye al daño citotóxico de los radicales. Otra hipótesis son los datos de que un modo de acción de 2u-globulina podría contribuir a la nefropatía inducida por HCE, pero no son suficientes. |
| Incompatibilidades | Incompatible con ácidos fuertes, oxidantes (cloratos, nitratos, peróxidos, permanganatos, percloratos, cloro, bromo, flúor, etc.); el contacto puede provocar incendios o explosiones. Mantener alejado de bases fuertes. |
| Eliminación de residuos | Incineración después de mezclar con otro combustible. Se debe tener cuidado para asegurar una combustión completa y evitar la formación de fosgeno. Es necesario un depurador de ácidos para eliminar los haloácidos producidos. Consulte con las agencias reguladoras ambientales para obtener orientación sobre prácticas de eliminación aceptables. Los generadores de desechos que contengan este contaminante (mayor o igual a 100 kg/mes) deben cumplir con las regulaciones de la EPA que rigen el almacenamiento, el transporte, el tratamiento y la eliminación de desechos. |
| Productos y materias primas para la preparación del hexacloroetano |
| Materias primas | Sodium hydroxide-->Chlorine-->Carbon tetrachloride-->Trichloroethylene-->Tetrachloroethylene-->1,1,2,2-Tetrachloroethane-->PENTACHLOROETHANE-->ACETYLTRIPHENYLGERMANE-->TRIPHENYLGERMANIUM CHLORIDE-->1,1,1-TRICLOROACETONA |
| Productos de preparación | METHYL-2-CHLOROOXAZOLE-5-CARBOXYLATE-->1,1,2-Trichlorotrifluoroethane-->2-Chloro-3-fluoropyridine-4-carboxylic acid-->1,2-DIFLUOROTETRACHLOROETHANE-->1,2-DICHLOROTETRAFLUOROETHANE-->Ethanediamide, N1,N1,N2,N2-tetraethyl--->DIMETHYLPHOSPHORAMIDOUS DICHLORIDE-->4-chloropyridine-->3-Cloroquinolina |
Etiqueta: Hexacloroetano, fabricantes, proveedores y fábricas de hexacloroetano en China
También podría gustarte
Envíeconsulta




