| Descripción |
Las cianopiridinas son las siguientes:{{0}}ciano-: Líquido o sólido de color blanco a tostado con olor a almendra. Punto de ebullición=alrededor de 213 grados; Punto de congelación/fusión=27 grado; Punto de inflamación=89 grado.3-ciano-: Líquido incoloro o sólido cristalino gris. Peso molecular=104.12; Punto de ebullición=83-84 grados; Punto de congelación/fusión=47-49 grados. Identificación de peligros (basado en el sistema de clasificación NFPA-704 M): Salud 3, Inflamabilidad 3, Reactividad 0. Soluble en agua.4-ciano-: Un sólido beige. Punto de congelación/fusión=75.8 grados |
| Propiedades químicas |
sólido cristalino de color blanco a marrón de bajo punto de fusión |
| Propiedades químicas |
Las cianopiridinas son las siguientes: 2-ciano-: líquido o sólido de color blanco a tostado. Olor a almendras. Punto de ebullición=2213 grado; punto de congelación/fusión=27 grados; punto de inflamación=89 grado. 3-ciano-: un líquido incoloro o un sólido cristalino gris. |
| Usos |
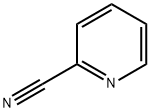
2-La cianopiridina es una piridina sustituida con ciano. 2-La cianopiridina es un compuesto relacionado de la nicotina y es un componente del condensado del humo del tabaco. |
| Usos |
Se emplea como un importante intermediario químico para el bromhidrato de rimiterol y como broncodilatador. También se utiliza como intermediario de productos farmacéuticos, colorantes y pigmentos. Actúa como precursor del respectivo amidato para la modificación de proteínas mediante amidación. |
| Definición |
ChEBI: una cianopiridina que lleva el grupo ciano en la posición 2. |
| Posible exposición |
Límites en el aire NIOSH IDLH525 mg/m3 NIOSH REL: (nitrilos) 2 ppm, concentración máxima, que no debe excederse en ningún período de trabajo de 15-minutos. |
| Primeros auxilios |
Si esta sustancia química entra en contacto con los ojos, quítese los lentes de contacto de inmediato e irrigue inmediatamente durante al menos 15 minutos, levantando ocasionalmente los párpados superior e inferior. Busque atención médica de inmediato. Si esta sustancia química entra en contacto con la piel, quítese la ropa contaminada y lávese inmediatamente con agua y jabón. Busque atención médica de inmediato. Si esta sustancia química ha sido inhalada, retírela de la exposición, comience la respiración boca a boca (usando precauciones universales, incluida la máscara de reanimación) si la respiración se ha detenido y la RCP si la actividad cardíaca se ha detenido. Traslade rápidamente a un centro médico. Cuando se haya ingerido este químico, busque atención médica. Dar grandes cantidades de agua e inducir el vómito. No hacer vomitar a una persona inconsciente. |
| almacenamiento |
Código de color azul: peligro para la salud/veneno: almacenar en un lugar seguro contra venenos. Antes de trabajar con este químico, debe recibir capacitación sobre su manejo y almacenamiento adecuados. Almacenar en recipientes bien cerrados en un área fresca y bien ventilada, lejos del calor o llamas y separado de materiales oxidantes. |
| Envío |
UN3276 Nitrilos, líquidos, tóxicos, nos, Clase de peligro: 6.1; Etiquetas: 6.1-Materiales venenosos, Nombre técnico requerido, Peligro potencial de inhalación (Disposición especial 5). |
| Incompatibilidades |
Agentes oxidantes, como percloratos, peróxidos y permanganatos. Los nitrilos pueden polimerizarse en presencia de metales y algunos compuestos metálicos. Son incompatibles con los ácidos; mezclar nitrilos con ácidos oxidantes fuertes puede provocar reacciones extremadamente violentas. Los nitrilos generalmente son incompatibles con otros agentes oxidantes como peróxidos y epóxidos. La combinación de bases y nitrilos puede producir cianuro de hidrógeno. Los nitrilos se hidrolizan tanto en ácido como en base acuosa para dar ácidos carboxílicos (o sales de ácidos carboxílicos). Estas reacciones generan calor. Los peróxidos convierten los nitrilos en amidas. Los nitrilos pueden reaccionar vigorosamente con agentes reductores. El acetonitrilo y el propionitrilo son solubles en agua, pero los nitrilos superiores al propionitrilo tienen baja solubilidad acuosa. También son insolubles en ácidos acuosos. |